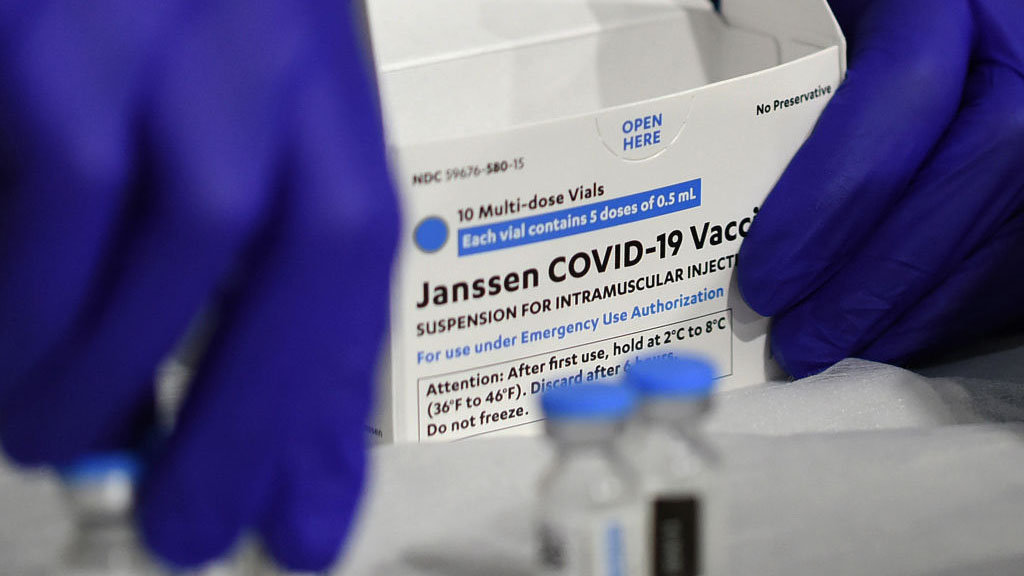
WASHINGTON - La Administración de Alimentos y Medicamentos de Estados Unidos (FDA, por sus siglas en inglés) dio luz verde este viernes a la reanudación "de inmediato" del uso de la vacuna de Janssen, filial belga de Johnson & Johnson, contra el COVID-19.
La decisión del organismo regulador llegó poco después de que un comité asesor de los Centros para el Control y la Prevención de Enfermedades (CDC, por sus siglas en inglés) aconsejase este mismo viernes retomar la vacunación con este suero, agregando una advertencia sobre posibles riesgos.
"Hemos concluido que los beneficios conocidos y potenciales de la vacuna (de Johnson & Johnson) contra el COVID-19 superan sus riesgos conocidos y potenciales en personas de 18 años o mayores", afirmó en una rueda de prensa la directora en funciones de la FDA, Janet Woodcock.
"Estamos seguros de que esta vacuna sigue cumpliendo con nuestros estándares de seguridad, eficacia y calidad", agregó.
Estados Unidos recomendó el pasado 13 de abril suspender el uso del suero después de que se detectaran seis casos de trombosis cerebral en mujeres menores de 48 años, de las que una falleció.
Manténte al tanto de las noticias locales y del estado del tiempo. Suscríbete a nuestros newsletters gratuitos aquí.
En la rueda de prensa, Woodcock aseguró que la posibilidad de que la trombosis cerebral ocurra "es muy baja", aunque dijo que la FDA y los CDC seguirán investigando su riesgo potencial.
A fecha de este viernes, las autoridades en Estados Unidos habían documentado 15 casos confirmados de trombosis cerebral en vacunadas con Johnson & Johnson en un abanico más amplio de edades y con un total de tres muertas entre los ocho millones de dosis administradas.